
このウェッブ版では、『リスク評価を読み解くハンドブック』の第1章「リスク評価の要素」(P.9)を
さらに詳しく説明しています。
まずは、有害性評価について、詳しくみていきましょう。
有害性評価では、有害性の可能性があるかないかを以下の手段で確認します。
まず、ヒトにおける知見(疫学のデータ)で、実際の生活の中での有害性を検討します。しかし、多くは、疫学データが不十分なため、実験によるデータでの評価を行います。
実験による評価では、一般毒性、発がん性、遺伝毒性などの有無が確認されます。特に、遺伝毒性の有無は、次のステップ②の用量・反応評価に影響を与えます。遺伝毒性の評価には Ames(復帰突然変異)試験(in vitro試験)、染色体異常試験(in vitro試験)、小核試験(in vivo試験)という代表的な 3つの試験が行われることが一般的です。
リスク評価の第2段階である用量・反応評価では、化学物質の摂取量(ばく露量)と有害影響の発生について、「量」からみた健康への影響度を見ます。
・有害性については、ヒトでの知見がない場合が多く、動物の毒性試験のデータから考察します。
・ リスクに対する考え方は、いき値(しきい値)が「ある」か「ない」かで、異なります。
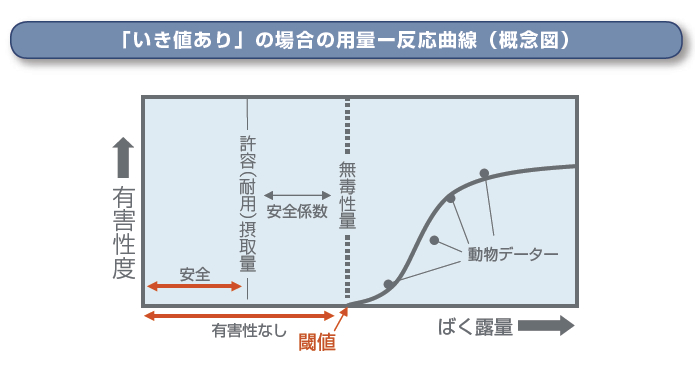
先に説明したように、ある量以下では有害性は生じない値が、「いき値」です。一般的な有害性や非遺伝毒性の発がん物質では、いき値があり、それ以下は問題ないというのが基本の考え方です。
しかしながら、その値は動物データから導いた値のため、安全係数(不確実係数)をかけ、さらに安全をみた値(許容摂取量)を設定します。
安全係数のとり方については、一般的に100倍(種差10倍×個人差10倍)を用いることが多いですが、重篤度や不確実性などを考慮し、ケースバイケースで 1000 ?10000 倍を用いることもあります。
そして、実際のばく露量がその許容(耐用)摂取量より小さければ、安全に問題ないと判断します。農薬や食品添加物は、この考え方に基づき規制が行われています。
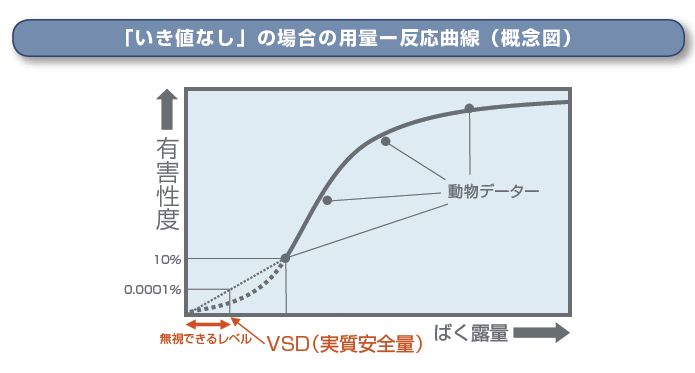
遺伝毒性発がん物質(DNA に損傷をきたすもの)では、たとえ微量でもあれば、遺伝子に直接作用し発がんを引き起こす可能性があると考えられ、そのばく露量がゼロにならない限り、発がんの可能性もゼロにならない、つまり、「いき値なし」と考えられています。
現実には、実際のヒトへの発がん性は、かなり少ない摂取量(低用量のばく露量)で発生していると考えられています。しかし、少ない量での影響をみるのは困難なので、動物実験では、ヒトが摂取する量より多い量(高用量のばく露量)で行われます。そのため現在ではより「安全側」の立場にたち、多くの場合、低用量域では、ゼロに向けて直線を引き、低用量での影響を評価する方法をとります。これを直線外挿法と呼びます。
なお、10 万分の 1(0.001%)や 100 万分の 1(0.0001%)の発がん率であれば、そのリスクは十分に小さく容認できるという考え方が、1970 年代より米国を中心に、国際的に受け入れられるようになってきました。この 10 万分の 1 や 100 万分の 1 のリスクレベルのばく露量の値を実質安全量(VSD)といい、それより小さければ、リスクは無視できるリスクとみなされます。この評価法は、日本を含め、大気汚染規制濃度や飲料水の水質基準の策定など、非意図的にばく露される化学物質の評価に現在多く使われています。










